Kanser Genetiği

Kanser genetik bir hastalıktır; yani, hücrelerimizin işleyişini, özellikle nasıl büyüyüp bölündüklerini kontrol eden genlerdeki değişikliklerden kaynaklanır. Bu değişikliklerden bazıları nesiller boyu aktarılmış ailesel kalıtım kaynaklı olabileceği gibi, başka bazıları sadece hasta dokudaki hücrelerde yeni ortaya çıkmış genetik farklılıklardır.
Kansere neden olan genetik değişiklikler şunlar olabilir:
hücreler bölünürken meydana gelen hatalar,
tütün dumanındaki kimyasallar ve güneşten gelen ultraviyole ışınları gibi çevredeki çeşitli kaynaklardan gelen zararlı maddelerin neden olduğu DNA hasarları,
ebeveynlerinizden gelen kalıtsal DNA.
Vücut normalde kanserli hale gelmeden önce DNA'sı hasar görmüş hücreleri ortadan kaldırır. Ancak vücut dokularının bunu yapma yeteneği bireyler yaşlandıkça azalır. Bu, ileri yaşlarda kanser riskinin daha yüksek olmasının nedenlerinden biridir. Her insanın kanseri, benzersiz bir genetik değişiklik kombinasyonuna sahiptir. Kanser büyümeye devam ettikçe, ek değişiklikler meydana gelecektir. Aynı tümör içinde bile farklı hücrelerde farklı genetik değişiklikler olabilir.
Kanserli dokunun genomunda mutasyon taramaları ve genom dizi analizleri yapılarak hasta bireyde dokuyu oluşturan hücrelerin moleküler özellikleri belirlenebilir ve böylece hastalık ile savaşta yenilikçi yaklaşımlar geliştirilebilir.
1. Kanser Genom Analizi
Kanser genomiği, DNA tam dizisinin ve DNA’nın tümör hücrelerindeki ifadesinin incelenmesi olarak tanımlanabilir. 2003 yılında insan genomunun dizilenmesi tamamlandıktan sonra gen havuzu hakkında elde edilen bilginin artmasıyla kanserin incelenme şeklinde farklı yöntemler geliştirilmeye başlanmıştır. Tüm genom analizi tümör örneklerinde kansere sebep olduğu tespit edilen genetik değişikliklerin bazıları, hücre büyümesini ve hücre ölümünü (apoptoz) düzenleyen ve genellikle kansere karşı koruyucu olan tümör baskılayıcı genlerin normal işleyişini bozmaktadır. Örneğin, tümör baskılayıcı genler BRCA1 ve BRCA2' deki mutasyonları barındıran kişilerin meme, yumurtalık ve prostat kanseri olma riskinin çok daha yüksek olduğu belirlenmiştir. Genetik mutasyonların tüm kanser tanılarında merkezi bir rolü olmasa da mutasyon varlığı veya yokluğu hastadaki kanserin tanımlanma şeklini değiştirebilmektedir. Ayrıca bazı genetik mutasyonlar tedavi seçimini de önemli ölçüde etkilemektedir.
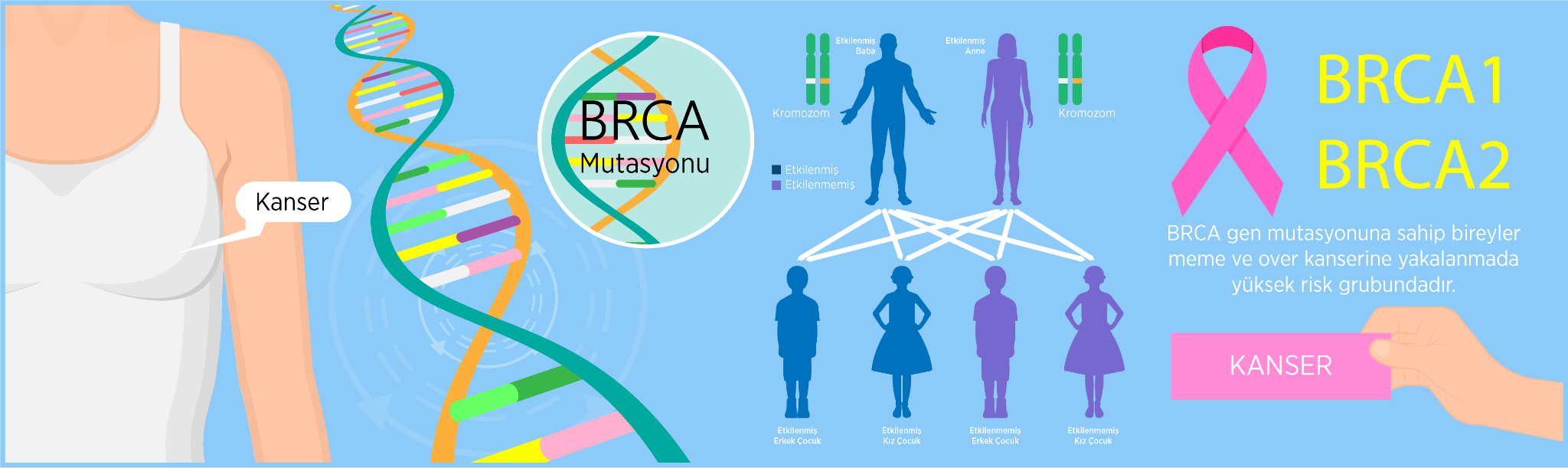
Genomik yaklaşım, yeni kanser ilaçlarının geliştirilmesini hızlandırmıştır. Kansere neden olan veya kanseri etkileyen genetik mutasyon ilaç geliştirme için potansiyel bir hedef olarak görülmektedir. Genler, hastalıklar ve ilaçlar arasındaki fonksiyonel bağlantıların keşfi için transkripsiyonel veriler oluşturulmuştur. Tespit edilen mutasyon noktaları sayesinde kanserin tedaviye dirençli hale gelme olasılığı ya da kullanılacak ilaca yanıt verip vermeyeceği belirlenmektedir.
Yeni nesil dizileme gibi yeni bilgi ve teknolojik gelişmelerin üretilmesiyle çok disiplinli ve karmaşık sistemler ile birlikte kanser üzerinde yapılan araştırmalar ilerlemeye devam edecektir.
Kişisel Tıp:
Hasta doku kaynaklı hücrelerin eldesi ve öncü ilaç kombinasyonlarının bu hücrelerde test edilmesi (insan dokuları taşıyabilen ksenograft hayvan, ve insan organoid doku modellerinin oluşturulması ve tedavide kullanılması).
Kişiselleştirilmiş kanser tedavisi, her hastaya özel bireysel tedaviler uygulanmasını tanımlayan bir kavramdır. Bireylerdeki ile birebir aynı özelliklere sahip kişiselleştirilmiş tümör modellerinin kullanılması, hastalarda ilaç yanıtlarının daha doğru tahmin edilmesine neden olabilir. Bireydeki hasta doku kaynaklı tümör organoid modelleri, hasta bireydeki tümörün moleküler ve hücresel bileşiminin korunması özelliği ile, geçmişte kullanılan modellere göre çeşitli avantajlara sahiptir. Bu avantajlar, kişiselleştirilmiş kanser tedavisinde, özellikle klinik öncesi ilaç taramasında ve seçilen tedavi rejimlerine hasta tepkilerini tahmin etmede tümör organoidlerinin etkileyici potansiyelini vurgulamaktadır.
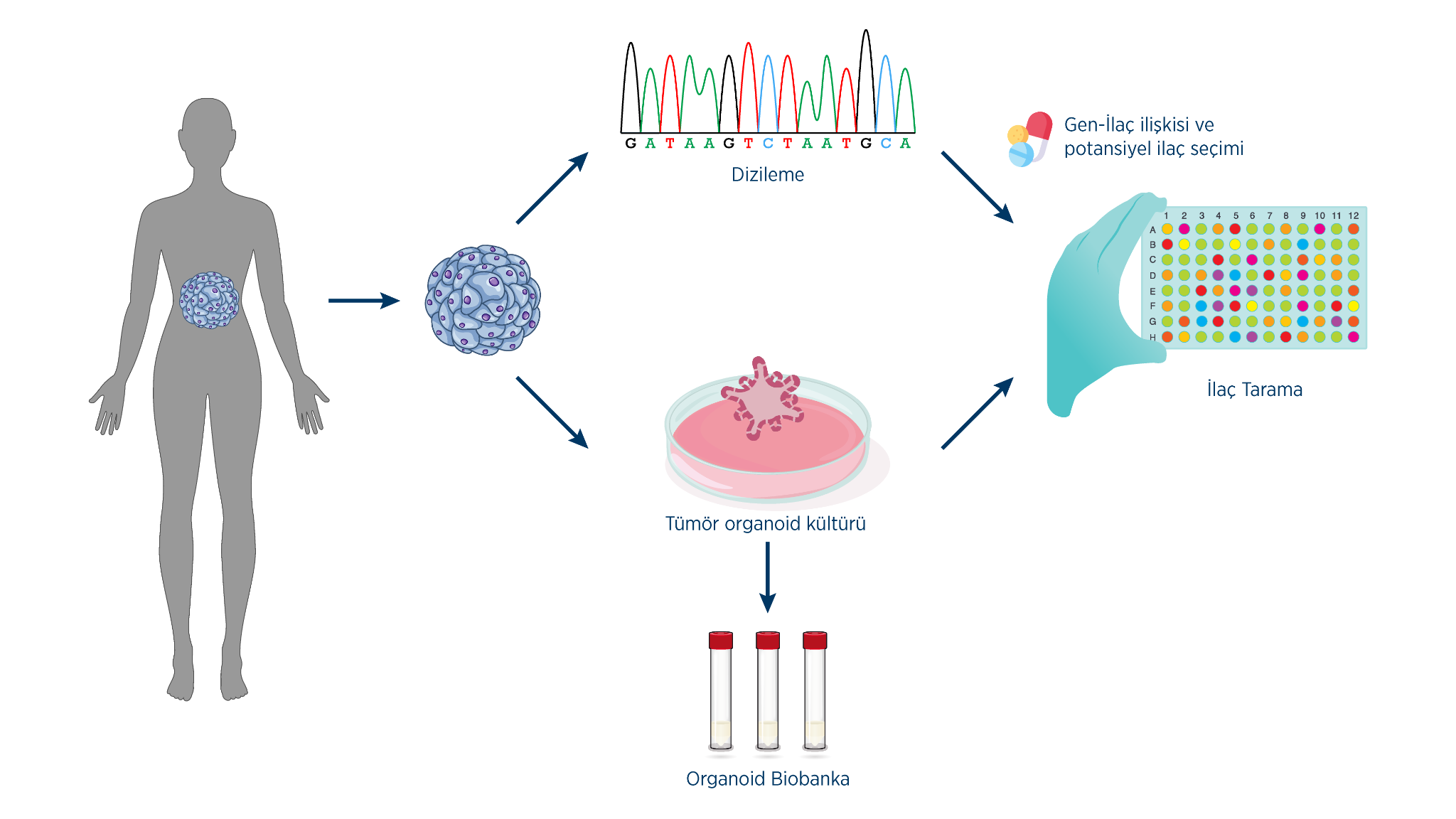
Şekil 1: Bu yaklaşımda prosedür, yeni nesil dizileme yöntemi kullanılarak tümör biyopsilerinin veya disseke örneklerin dizilenmesi ile başlar ve ilaç taramasına tabi tutulmadan önce primer tümörlerle histolojik ve patolojik olarak karşılaştırılacak olan hasta kaynaklı tümör organoidlerinin kültürü ile devam eder. Paralel olarak, türetilen organoidlerin bir kısmı bir biyobankalanarak korunacaktır. Sıralama sonuçlarına ve gen-ilaç ilişkilendirme bağlantılarına dayalı olarak etkili terapötik stratejileri belirlemek için, standart kemoterapi ve hedefe yönelik terapi etkenlerini içeren aday ilaçların yüksek verimli ilaç taramaları tekrar edilebilir bir süreçte gerçekleştirilebilir.
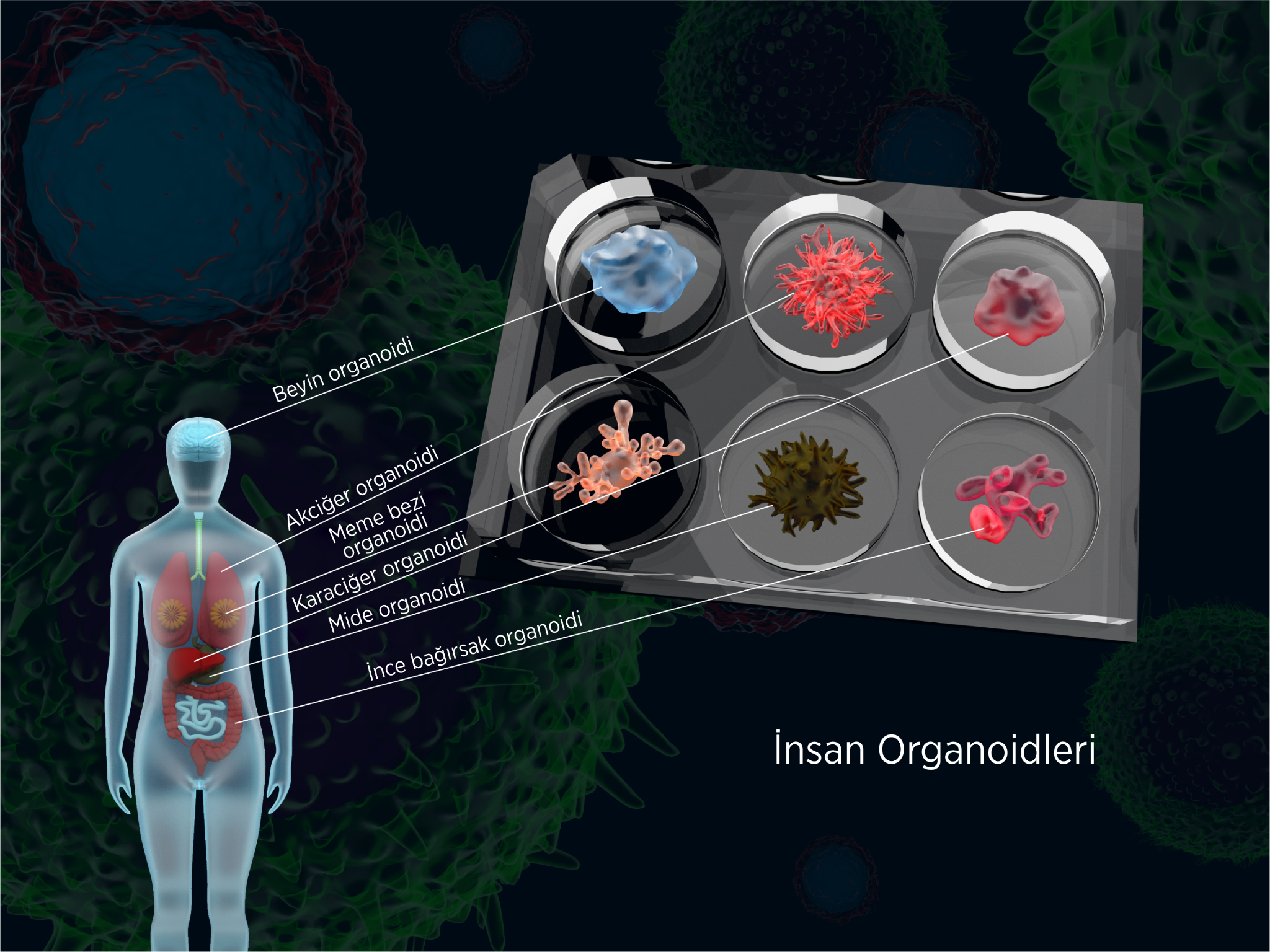
Şekil 2: İnsanda organoid geliştirme örnekleri (Es, H. A., Montazeri, L., Aref, A. R., Vosough, M., & Baharvand, H. (2018). Personalized cancer medicine: an organoid approach. Trends in biotechnology, 36(4), 358-371.’dan türkçelendirilmiştir.)Şekil 2: İnsanda organoid geliştirme örnekleri (Es, H. A., Montazeri, L., Aref, A. R., Vosough, M., & Baharvand, H. (2018). Personalized cancer medicine: an organoid approach. Trends in biotechnology, 36(4), 358-371.’dan türkçelendirilmiştir.)







